[코스인코리아닷컴 김민석 기자] 식약처는 홈페이지에 ‘의약외품 규제동향 인포허브’ 페이지를 신설하고 치약제에 대한 해외 규제정보(e-book)을 12월 31일부터 게시한다고 밝혔다. (식약처 누리집 > 정책정보 > 의료제품 수출지원 정보 > ‘의약외품 해외규제 인포허브’(신설)

규제정보는 해외 주요국별 치약제 관리 체계를 상세히 담고 있으며, 주요 내용은 ▲ 국가별 규제기관·품목 분류(의약품·의약외품·화장품 등) ▲ 인·허가 절차(치약 등록 시 제출자료, 치약 표준제조기준(monograph), 제품 표시 사항 등) ▲ 제조 및 품질 관리 기준(GMP) 적용 현황·사후 관리 제도 ▲ 관련 규정 등이다.
업계의 정보 활용도를 높이기 위해 국가별 품목 분류 및 표시사항 비교표를 수록하였고, 관련 규정의 원문을 바로 확인할 수 있도록 정보출처와 URL을 함께 제공했다. 자료 접근성과 활용성을 높이기 위해 전자책(e-book) 형태로 제작했다는 설명이다.
치약제는 의약외품 제품군 중 생산 실적이 가장 높은 제품군(’24년 기준 4,051억원)이며, 수출 실적 상위 국가는 중국(1위) > 영국(2위) > 일본(3위) 순으로 전체 수출 시장의 50% 이상을 차지한다. (‘24년 치약제 수출실적 : (전체) 471억원, △ 중국 133억원 △ 영국 58억원 △ 일본 57억원)
한국의약품수출입협회 류형선 회장은 “치약제는 미국은 의약품, 유럽은 화장품, 일본은 의약부외품으로 허가절차, 품질관리, 표시사항 등이 국가별로 규제 기준이 달라, 기업 입장에서는 그간 어려움이 있었다”며, “식약처에서 제공하는 해외 주요국의 규제동향은 국내 업계가 글로벌 시장 진출에 유용한 자료로 많은 도움이 될 것으로 기대한다.”고 말했다.
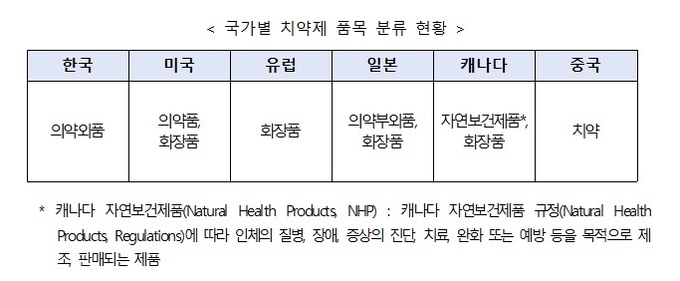
식약처는 같은 치약제라도 국가별로 제품 분류나 관리체계가 다르므로, 수출 시 해당 수출국 규제를 반드시 확인할 것을 당부했다.
업계에서는 화장품법의 ‘화장품 정의’에 ‘구강 점막’을 추가해 ‘화장품’으로 분류해달라는 의견을 제기하고 있다. 차제에 치약을 화장품으로 분류하는 안의 적극적인 검토가 필요해 보인다.




![[AI의 종목 이야기] '2026년 국고보조금' 정책 발표, 스마트안경 최초 포함](https://img.newspim.com/etc/portfolio/pc_portfolio.jpg)

