경구용 수면무호흡증 치료제 개발사
2상 임상시험 성공, 바로 3상 돌입
대부분이 양압기 의존, 낮은 순응도
"양압기 거부 환자에 최적 선택지"
이 기사는 8월 7일 오후 3시50분 '해외 주식 투자의 도우미' GAM(Global Asset Management)에 출고된 프리미엄 기사입니다. GAM에서 회원 가입을 하면 9000여 해외 종목의 프리미엄 기사를 보실 수 있습니다.
[서울=뉴스핌] 이홍규 기자 = 미국에 상장된 임상시험 단계의 의약품 개발업체 인캔넥스헬스케어(종목코드: IXHL)의 인기가 우리나라 투자자 사이에서 상당하다.
최근 인캔넥스는 전 세계에 9억명이 앓는 수면무호흡증 치료제의 임상시험(2상)에서 긍정적 결과를 얻어 바로 개발 후기 단계에 돌입했다.
◆2상 시험 성공
한국예탁결제원에 따르면 6일까지 한 주 동안 인캔넥스 주식 순매수액은 약 1742만달러(약 241억원)로 상장지수펀드(ETF)를 포함한 미국 주식 순매수액 상위 50위권(23위)을 기록했다.
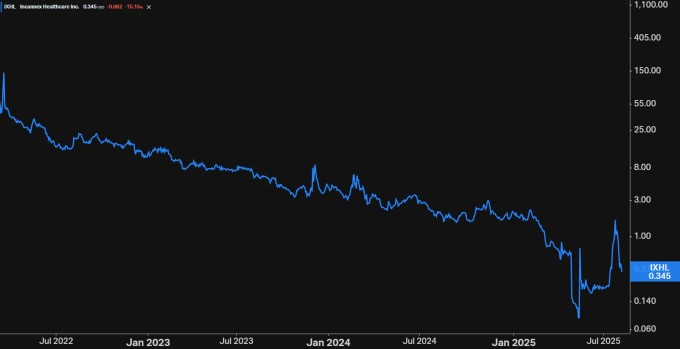
인캔넥스는 호주의 의약품 개발회사다. 당초 주상장처를 호주증권거래소에 두고 미국 나스닥에도 예탁증권(ADR)을 상장(2022년 2월)한 이중 상장 형태로 존재했다가 2023년 11월 소재지 변경을 통해 아예 나스닥에만 상장한 기업이 됐다.
인캔넥스가 최근 우리나라 투자자 사이에서 인기를 끈 것은 지난달 30일 공개된 폐쇄성 수면무호흡증(OSA) 치료용 신약 후보물질 'IHL-42X'의 2상 임상시험 최종 결과가 계기가 됐다.
관련 시험(중증 성인 121명 대상)에서 고용량뿐 아니라 저용량 투여군 모두에서 OSA 증상이 투여 전 대비 크게 감소해 임상적으로 긍정적인 결과를 냈다. 저용량군에서 평균 51% 감소했고, 또 환자의 25%가 80%가 넘는 감소를 경험했다고 했다. 심각한 부작용은 관찰되지 않았다고 한다.
◆경구용 치료제
IHL-42X가 주목되는 것은 경구용으로 개발되고 있어서다. 관련 약물을 개발 중인 경쟁사로는 앱니메드(Apnimed)가 있지만 현재까지 의약당국의 승인을 얻은 OSA 치료 방법 중에서 경구용 약물 복용은 없는 상태다.
현재 OSA를 앓고 있는 환자 대부분이 양압기로 불리는 'CPAP'로 치료 처방을 받지만 순응도가 낮다. 매일 밤 마스크를 착용하고 압력이 가해진 공기를 들이마시며 자는 것 자체가 불편한 데다가 마스크를 3~6개월마다 교체해야 하는 번거로움도 있어서다.

따라서 경구용 OSA 치료제는 CPAP 사용의 불편함과 번거로움을 겪는 환자들에게 유인력을 가질 가능성이 크다. 예로 현재 수면무호흡증 시장에서 CPAP 기기의 점유율은 74%지만 60~80% 환자가 장기 사용을 중단하는 것으로 파악됐다.
인캔넥스의 IHL-42X가 승인되면 당장 미국에서만 30억달러에 가까운 기회가 생긴다. 현재 미국에서 CPAP 장기 사용 중단이나 치료 실패, 치료법 접근 불가에 의해 형성된 미충족 시장은 약 28억달러로 추산된다.
경구용 치료제가 기존 CPAP 환자 사이에서도 널리 채택되면 그 규모는 더욱 커질 가능성이 있다. 현재 세계 9억명, 미국인 3000만명이 OSA을 앓는 가운데 2035년까지 세계 시장 규모는 40억달러에 도달할 것으로 전망된다.
◆승인 낙관론
전문가 사이에서 IHL-42X의 최종 승인 가능성은 비교적 높은 편으로 평가된다. 임상시험 결과가 우수하다는 평가를 받는 가운데 최근 수면의학계 저명한 전문가인 더글라스 B. 커쉬 박사를 자사의 임상자문위원회로 합류시켜 3상 시험의 신뢰도를 높였다.
또 현재까지 FDA가 승인한 OSA 치료 약물은 일라이릴리의 체중감량 치료제로 널리 알려져 있는 '제프바운드' 하나 뿐인데 이마저도 OSA 치료용으로는 비만 환자에게만 쓸 수 있어 일반 OSA 환자에는 대안이 부재한 상황이다.
최종 결과도 비교적 조기에 나올 가능성도 거론된다. 내후년 승인 가능성이 언급된다. 지난 5월 이미 FDA로부터 3상 임상시험의 프로토콜을 승인받아 즉시 3상 시험에 착수한 가운데 전통적인 신약 신청 경로 '505(b)(1)'이 아닌 '505(b)(2)'를 택했다.
505(b)(2) 경로를 통한 개발은 이전에 승인된 약물의 공개된 안전성이나 효능 데이터를 참조할 수 있어 개발 시간과 비용을 크게 줄일 수 있다. IHL-42X는 드로나비놀(1985년 승인)과 아세타졸아마이드(1953년 승인)라는 두 약물을 활용하는 것이다.
▶②편에서 계속
bernard0202@newspim.com


![‘케데헌’ 열풍에 커지는 굿즈 시장…사모펀드 투자도 확산[시그널]](https://newsimg.sedaily.com/2025/08/06/2GWIRYS16D_1.jpg)

![릴리 '경구용 비만약' 3상 결과에 일동제약 주가 쑥 [Why 바이오]](https://newsimg.sedaily.com/2025/08/08/2GWJNYQYVO_1.jpg)
![[GAM] 아스테라 랩스의 질주 ① AI 연결성 솔루션의 선두주자](https://img.newspim.com/news/2025/08/08/2508080235019410.jpg)
