기초과학연구원(IBS·원장 노도영) 연구진이 자폐 환자에 동반되는 불안, 공포 장애 기전을 밝혀냈다. 자폐 환자의 PTSD 치료법 개발에 한 발 다가섰다.
IBS는 김은준 시냅스 뇌질환 연구단장(KAIST 생명과학과 석좌교수)팀이 자폐 환자에게서 발견된 것과 같은 유전자 변이를 지닌 생쥐 실험을 통해, '기저편도체' 흥분성 신경세포 활성 조절이 공포 기억 소거와 공포 반응 억제 핵심 역할을 함을 규명했다고 17일 밝혔다.
기저편도체는 감정 조절과 공포 기억 소거에 중요 역할을 하는 뇌 부위다. 공포 기억 소거는 반복된 공포 자극 노출로, 공포 반응이 점차 줄어드는 과정이다.
연구팀은 자폐와 PTSD 증상 기전을 이해하기 위해 뇌 발달 및 시냅스 가소성 조절 핵심 인자인 'NMDA 수용체'(NMDAR)에 주목했다. 이 수용체 구성 요소 중 하나인 GluN2B 단백질은 발달 초기에 뇌 회로 형성·유지에 중요한 역할을 하는데, GluN2B를 만드는 '설계도' 격인 GRIN2B 유전자 변이는 다양한 뇌·정신질환과 연관된 것으로 알려져 있다.
연구진은 이런 GRIN2B 유전자의 C456Y 변이를 가진 생쥐를 대상으로 실험을 진행, 이 생쥐가 위협적 상황을 겪은 뒤 시간이 지나도 PTSD 증상을 나타냄을 확인했다.
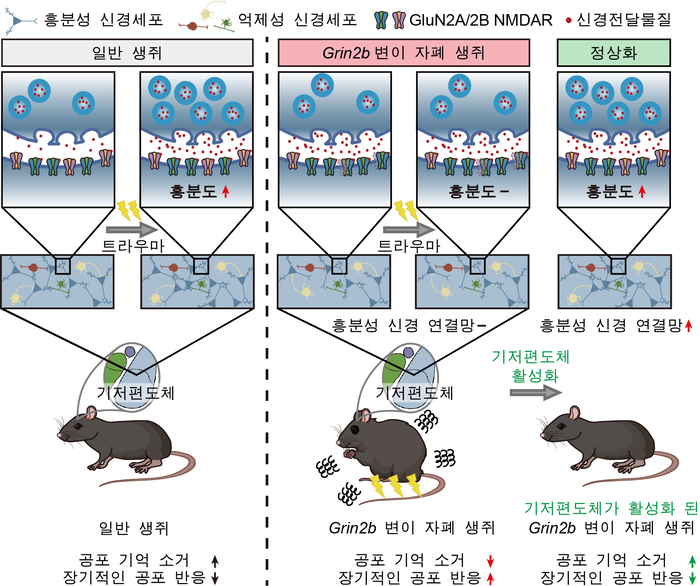
추가 연구와 분석에서는 변이 생쥐의 기저편도체가 트라우마 이후 충분히 활성화되지 않고, 이 부위 흥분성 신경세포가 장기간 억제돼 있음이 확인됐다.
더욱이 변이 생쥐의 기저편도체 흥분성 신경세포를 인위적으로 활성화시키자, 억제된 신경 전달과 흥분성이 정상화됐다. 공포 기억은 소거되고 장기적인 공포 반응도 완화됐다. 기저편도체 비활성화가 포 반응의 핵심 원인이었음을 시사하는 결과다.
김은준 단장은 “이번 연구는 자폐 환자에게서 나타나는 PTSD 유사 증상 원인이 기저편도체에 있는 흥분성 신경세포 장기 억제에 있음을 세포, 시냅스, 뇌 회로 수준에서 최초로 규명한 성과”라며 “이는 기저편도체의 활성이 향후 자폐 환자의 PTSD 관련 치료 전략 개발에 중요한 단서를 제공할 수 있다”고 말했다.
연구 결과는 국제학술지 '사이언스 어드밴시스'에 17일(현지시간) 온라인 게재됐다.
김영준 기자 kyj85@etnews.com

![[K-항암 프로젝트]〈2〉RACE, 면역항암제도 못 잡는 콜드 튜머…AI·오가노이드로 뚫는다](https://img.etnews.com/news/article/2025/09/17/news-p.v1.20250917.40e3a2e28828430d913e580e852071dc_P1.png)




